Leptospiras recuperadas de aguas superficiales del noreste de la provincia de La Pampa
Leptospires recovered from surface waters of the northeast of La Pampa province
DOI:
https://doi.org/10.19137/cienvet.v28.9770Palabras clave:
Leptospirosis, aislamiento, climas templados, PCR, agua de lluvia, humedalesResumen
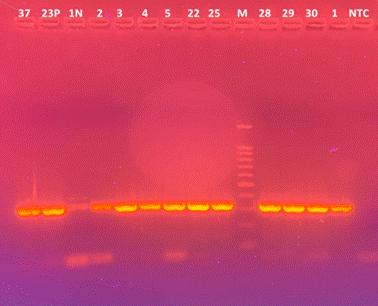
La leptospirosis es una zoonosis bacteriana de distribución mundial, producida por espiroquetas del género Leptospira. La incidencia de la enfermedad es mayor en climas cálidos y húmedos y los brotes estacionales son frecuentes después de inundaciones. Los animales domésticos y silvestres actúan como reservorios y eliminan leptospiras por la orina produciendo contaminación del medio ambiente. La asociación entre el contacto con el agua ambiental y el riesgo de infección por Leptospira en climas templados no está totalmente claro. El objetivo del presente trabajo fue determinar la presencia de leptospiras patógenas y no patógenas en aguas ambientales de la región noreste de la provincia de La Pampa mediante el aislamiento por cultivo y la posterior identificación de las genomoespecies mediante técnicas de biología molecular. El muestreo se efectuó después de los episodios de precipitación pluvial, en el período septiembre 2021–marzo 2025, registrándose meses con muy pocas precipitaciones. Se procesaron 86 muestras de agua de canales pluviales y humedales. Se recuperaron espiroquetas en el 10,5% (n=9) de las muestras. Ninguna de las cepas recuperadas presentó el gen lipL32 característico de las especies patógenas. Mediante la secuenciación parcial del gen 16S rARN se determinaron las genomoespecies: Leptospira ellinghausenii/Leptospira yanagawae/Leptospira.meyeri (n=5), Leptospira idonii (n=2), Leptospira vanthielii (n=1), Leptospira fainei (n=1). Todas pertenecen al grupo saprófitas excepto L.fainei, incluida en el subclado P2 (grupo intermedias). Es necesario aplicar técnicas moleculares de última generación en conjunto con la determinación del serovar para poder identificar correctamente a las espiroquetas aisladas de aguas superficiales y así estimar su potencial riesgo para la salud humana y animal
Descargas
Citas
Levett PN. Leptospirosis. Clin Microbiol Rev. 2001. 14(2):296-326. https://doi.org/10.1128/CMR.14.2.296-326.2001
Levett PN. Systematics of Leptospiraceae. En Leptospira and Leptospirosis, ed. por Adler B, 11-20. Curr Top Microbiol Immunol. 2015; 387. Berlin, Heidelberg: Springer.
Hamond C. et al Isolation and characterization of saprophytic and pathogenic strains of Leptospira from water sources in the Midwestern United States. Front Water. 2024. 6:1278088. Disponible en https://doi.org/10.3389/frwa.2024.1278088
Ahmed N et al. Multilocus sequence typing method for identification and genotypic classification of pathogenic Leptospira species. Ann Clin Microbiol Antimicrob. 2006. 5, 28. Disponible en: https://doi.org/10.1186/1476-0711-5-28
Vincent AT. et al. Revisiting the taxonomy and evolution of pathogenicity of the genus Leptospira through the prism of genomics. PLoS Negl Trop Dis. 2019.23;13(5), e0007270. Disponible en: https://doi.org/10.1371/journal.pntd.0007270
Bradley EA, Lockaby G. Leptospirosis and the Environment: A Review and Future Directions. Pathogens (Basel, Switzerland), 2023. 12(9), 1167. Disponible en https://doi.org/10.3390/pathogens12091167
Asociación Argentina De Veterinarios De Laboratorio (AAVLD) 2017. Informe sobre Leptospirosis. Comisión Científica de leptospirosis. http://www.aavld.org.ar/documentos/6-INFORME%20SOBRE%20LEPTOSPIROSIS%20%202016.pdf
Sadler E, Vallee E, Watts J, Wada M. The effects of rain and flooding on leptospirosis incidence in sheep and cattle in New Zealand. New Zealand Vet J, 2025. 1–13. Disponible en https://doi.org/10.1080/00480169.2025.2540324
Muñoz-Zanzi C, Mason MR, Encina C, Astroza A, Romero A. Leptospira contamination in household and environmental water in rural communities in southern Chile. Int J Environ Res Public Health. 2014.11:6666–80. Disponible en https://doi.org/10.3390/ijerph110706666
Hartskeerl RA, Collares-Pereira M, Ellis WA. Emergence, control and re-emerging leptospirosis: dynamics of infection in the changing world. Clin Microbiol Infect. 2011. 17(4):494-501. Disponible en https://doi.org/10.1111/j.1469-0691.2011.03474.x
Licoff N, Koval A, López S, Margueritte J, Mejía M. Brote de leptospirosis en feed lot: descripción del caso, confirmación diagnóstica y medidas de control implementadas. Vet Arg. 2008. 25(250):749-755
Koziol EE, Moliner AI, Vanasco NB, Scala MR, Signorini M, Tarabla H. Conocimiento de zoonosis en operarios tamberos de la provincia de Santa Fe, Argentina. In Vet. 2016.18(1): 45-52.
Koval A, López S, Lagioia G, Bertino R, Romera MR, Scialfa E. Brote de leptospirosis en bovinos y humanos en un tambo de Lincoln, Provincia de Buenos Aires. Vet. Arg.2017, 34(355).
Koval AA, Brihuega BF, Loffler SG, López S, Martin MS, Lagioia GG, Insaugarat JR. Primer aislamiento de Leptospira borgpetersenii serovar Hardjo tipo Hardjo Bovis a partir de un caso clínico en Argentina. Rev Argent Microbiol. 2020, 52(3), 61-70. Disponible en: https://www.scielo.org.ar/scielo.php?script=sci_arttext&pid=S0325-75412020000300061&lng=es.
Vanasco B, Benegas L, Uboldi A, Lanzotti M, Flynn L, Sardi F, Rodríguez Alassia P. 2016. Capítulo de Leptospirosis en: Consenso Sobre Enfermedades Infecciosas
Regionales En La Argentina Recomendaciones de la Sociedad Argentina de Pediatría- Comité Nacional de Infectología. http://www.anlis.gov.ar/iner/?page_id=1193
Heydari P, Tirbandpay M, Ghasemishayan R. Systematic review of the prevalence of environmental and host-related risk factors and the zoonotic potential of leptospirosis in domestic dogs in regions impacted by environmental changes. BMC Vet Res, 2025. 21(1), 564. Disponible en https://doi.org/10.1186/s12917-025-05023-0
Rajaonarivelo JA et al. Leptospira prevalence and lineages vary across land-use types due to shifts in small mammal communities. Appl Environ Microbiol. 2026. e0206125. Disponible en: https://doi.org/10.1128/aem.02061-25
Colombo VC, Gamietea I, GruneLoffler S, Brihuega B, Beldomenico PM. New host species for Leptospira borgpetersenii and Leptospira interrogans serovar Copenhageni. Vet Microbiol. 2018. 215:90-2. Disponible en: https://doi.org/10.1016/j.vetmic.2018.01.007
Kin MS, Brihuega B, Fort M, Delgado F, Bedotti D, Casanave EB. Presence of antibodies against Leptospira serovars in Chaetophractus villosus (Mammalia, Dasypodidae), La Pampa province, Argentina. Rev Argent Microbiol. 2015, 47(1):41-6. Disponible en: https://doi.org/10.1016/j.ram.2015.01.005
Kin MS et al. First record of the presence of antibodies against Leptospira in Lagostomus maximus, and Leptospira weillii serogroup Celledoni in Chaetophractus villosus, Argentina. Comp Immunol Microbiol Infect Dis, 2025. 117,102302. Disponible en: https://doi.org/10.1016/j.cimid.2025.102302
Yanagihara Y et al. Leptospira Is an Environmental Bacterium That Grows in Waterlogged Soil. Microbiol. Spectr. 2022, 10, e02157-21 Disponible en https://doi.org/10.1128/spectrum.02157-21
Chakraborty A, Miyahara S, Villanueva SY, Saito M, Gloriani NG, Si Y. A novel combination of selective agents for isolation of Leptospira species. Microbiol Immunol. 2011.55, 494–501. Disponible en: doi: 10.1111/j.1348-0421.2011.00347.x
Zulkifli NF, Wan SJ, Neela VK, Chee HY, Masri SN, et al. Detection of Leptospira Species in Environmental Samples by Amplification of 16S rRNA and rpoβ Genes. Sains Malaysiana 2018. 47: 1795– 1800.
Thibeaux R et al. Biodiversity of Environmental Leptospira: Improving Identification and Revisiting the Diagnosis. Front Microbiol. 2018 9:816. Disponible en: doi: 10.3389/fmicb.2018.00816
Levett PN, Morey RE, Galloway RL, Turner DE, Steigerwalt AG, et al. Detection of pathogenic leptospires by real-time quantitative PCR. J Med Microbiol. 2005, 54: 45–49. Disponible en: https://doi.org/10.1099/jmm.0. 45860-0
Bierque E, Thibeaux R, Girault D, Soupe´- Gilbert M-E, Goarant C. A systematic review of Leptospira in water and soil environments. PLoS ONE. 2020. 15(1): e0227055. Disponible en https://doi.org/10.1371/journal.pone.0227055
Francois BS, Brihuega FB, Grune LS, Gattarello MV, Correa PD, Petrakovsky MJ, Gualtieri SC, Arestegui LM. Isolation of Leptospira borgpetersenii in water sources in Argentina. Rev Cubana Med Trop. 2013;65(2):177-184.
Grune Loffler S et al. Detección de Leptospira spp. (Spirochaetales: Leptospiraceae) en muestras ambientales de regiones habitadas por poblaciones vulnerables del norte argentino. Revista FAVE. Sección Ciencias veterinarias, 2021. 20(2), 91-96. Disponible en https://doi.org/https://doi.org/10.14409/favecv.v20i2.10119
Martin LP. Diagnóstico de leptospirosis canina mediante una técnica de PCR en tiempo real. 2018. Tesis de Doctorado. Facultad de Ciencias Veterinarias. Universidad Nacional de La Plata.
Villumsen S, Pedersen R, Borre MB, Ahrens P, Jensen JS, Krogfelt KA. Novel TaqMan® PCR for detection of Leptospira species in urine and blood: pit-falls of in silico validation. J Microbiol Methods. 2012.91(1):184-90. Disponible en: https://doi.org/10.1016/j.mimet.2012.06.009
Merien F, Amouriaux P, Perolat P, Baranton G, Saint Girons I. Polymerase chain reaction for detection of Leptospira spp. in clinical samples. J Clin Microbiol. 1992.30(9):2219–24. Disponible en: https://doi.org/10.1128/jcm.30.9.2219-2224.1992
Zarantonelli L et al. Isolation of pathogenic Leptospira strains from naturally infected cattle in Uruguay reveals high serovar diversity, and uncovers a relevant risk for human leptospirosis. PLoS Negl Trop Dis, 2018. 12(9): e0006694. https://doi.org/10. 1371/journal.pntd.0006694.
Jacob P, Chiani Y, Schmeling MF, Landolt N, Pujato N, Vanasco B. Leptospirosis humana en Argentina: un esquema de análisis, 2014. Rev Argent Salud Pública.2017;8(32):13-8. Disponible en: https://rasp.msal.gov.ar/index.php/rasp/article/view/114
Vanasco NB, Schmeling MF, Lottersberger J, Costa F, Ko AI, Tarabla HD. Clinical Characteristics and Risk Factors of Human Leptospirosis in Argentina (1999-2005). Acta Trop. 2008;107(3):255-8
Samrot AV, Sean TC, Bhavya KS, Sahithya CS, Chan-drasekaran S, Palanisamy R, Robinson ER, Subbiah SK, Mok PL. Leptospiral Infection, Pathogenesis and Its Diagnosis—A Review. Pathogens 2021, 10, 145. Disponible en: https://doi.org/10.3390/ pathogens10020145
Servicio meteorológico Nacional. Boletín Climatológico Anual (2023) https://ws2.smn.gob.ar/boletines/bolet%C3%ADn-climatol%C3%B3gico-anual-2023
Ministerio de Salud de la República Argentina, Dirección de Epidemiologia. (2025). Boletín Epidemiológico Nacional N°747, SE 10.
Scialfa E, Grune S, Brihuega B, Aguirre P, Rivero M. Isolation of saprophytic Leptospira spp. from a selected environmental water source of Argentina. Rev Argent Microbiol 2018; 50: 323–326. Disponible en: https://doi.org/10.1016/j.ram.2017.08.003
Gorman M, Xu R, Prakoso D, Salvador LCM, Rajeev S. Leptospira enrichment culture followed by ONT metagenomic sequencing allows better detection of Leptospira presence and diversity in water and soil samples. PLoS Negl Trop Dis. 2022 16(10): e0010589. https://doi.org/10.1371/journal.pntd.0010589
Narkkul U et al.Optimization of Culture Protocols to Isolate Leptospira spp. from Environmental Water, Field Investigation, and Identification of Factors Associated with the Presence of Leptospira spp. in the Environment. Trop Med Infect Dis. 2020, 5, 94. Disponible en : https://doi.org/10.3390/tropicalmed5020094
Kaboosi H, Razavi MR. Efficiency of Filtration Technique for Isolation of Leptospires from Surface Waters: Role of Different Membranes with Different Pore Size and Materials. Afr J Microbiol Res. 2010, 4, 671–676. 78.
Bharti AR, et al. Gilman RH, Willig MR, Gotuzzo E. Leptospirosis: a zoonotic disease of global importance. Lancet Infect Dis 2003. 3 (12): 757-71. Disponible en: https://doi.org/10.1016/s1473-3099(03)00830-2
Yasuda PH, Steigerwalt AG, Sulzer KR, Kaufmann AF, Rogers F, Brenner DJ. Deoxyribonucleic Acid Relatedness between Serogroups and Serovars in the Family Leptospiraceae with Proposals for Seven New Leptospira Species. Int J Syst Bacteriol., 1987, p. 407-15. Disponible en: https://doi.org/10.1099/00207713-37-4-407
Postic D, Riquelme-Sertour N, Merien F, Perolat P, Baranton G. Interest of partial 16S rDNA gene sequences to resolve heterogeneities between Leptospira collections: application to L. meyeri. Res Microbiol. 2000. 151,333–341. Disponible en: http://dx.doi.org/10.1016/S0923-2508(00)00156-X
Chiani Y et al. Isolation and clinical sample typing of human leptospirosis cases in Argentina. Infect Genet Evol. 2016;37:245-51. Disponible en: https://doi.org/10.1016/j.meegid.2015.11.033
Xu Y et al. Whole genome sequencing revealed host adaptation-focused genomic plasticity of pathogenic Leptospira. Sci Rep 6. 2016. Disponible en: https://doi.org/10.1038/srep20020
Lehmann JS, Matthias MA, Vinetz JM, Fouts DE. Leptospiral Pathogenomics. Pathogens. 2014; 3(2):280-308.Disponible en: https://doi.org/10.3390/pathogens3020280
Petersen AM, Boye K, Blom J, Schlichting P, Krogfelt KA. First isolation of Leptospira fainei serovar Hurstbridge from two human patients with Weil's syndrome. J Med Microbiol. 2001;50(1):96-100. doi: 10.1099/0022-1317-50-1-96.
Perolat P et al. Leptospira fainei sp. nov., isolated from pigs in Australia. Int J Syst Bacteriol. 1998. 48 Pt 3:851-8. doi: 10.1099/00207713-48-3-851.
Stagnoli A, House RV, Hagemann J, Dohmann K, Pfeffer M, Albrecht C. Seroprevalence of 16 Leptospira Serovars in Wild Boar (Sus scrofa) Hunted in Saxony-Anhalt, Germany. Animals (Basel). 2025.18;15(18):2725. https://doi.org/10.3390/ani15182725
Descargas
Publicado
Número
Sección
Licencia
Derechos de autor 2026 Claudia Tortone, Andrea Belen Schenheiter, Ana Inés Portu, Marisa Etel Giménez, Franco Exequiel Lucero Arteaga, María Lorena Marengo, Lorena Fernandez, Paula Lorena Martin, Delia Susana Oriani

Esta obra está bajo una licencia internacional Creative Commons Atribución-NoComercial-CompartirIgual 4.0.
Al momento de enviar sus contribuciones, los colaboradores deberán declarar , de manera fehaciente, que poseen el permiso del archivo o repositorio donde se obtuvieron los documentos que se anexan al trabajo, cualquiera sea su formato (manuscritos inéditos, imágenes, archivos audiovisuales, etc.), permiso que los autoriza a publicarlos y reproducirlos, liberando a la revista y sus editores de toda responsabilidad o reclamo de terceros , los autores deben adherir a la licencia Creative Commons denominada “Atribución - No Comercial CC BY-NC-SA”, mediante la cual el autor permite copiar, reproducir, distribuir, comunicar públicamente la obra y generar obras derivadas, siempre y cuando se cite y reconozca al autor original. No se permite, sin embargo, utilizar la obra con fines comerciales.






.jpg)

4.png)


7.png)






