Compartir Igual) a menos que se indique lo contrario, .http://www.creativecommons.org.ar/licencias.html
DOI: http://dx.doi.org/10.19137/cienvet202224207
![]() Esta obra se publica bajo licencia Creative Commons 4.0 Internacional. (Atribución-No Comercial-
Esta obra se publica bajo licencia Creative Commons 4.0 Internacional. (Atribución-No Comercial-
Compartir Igual) a menos que se indique lo contrario, .http://www.creativecommons.org.ar/licencias.html
COMUNICACIÓN CORTA
Guía para el uso del inmunodiagnóstico en ovinos
aplicado a la vigilancia epidemiológica de la
equinococosis quística
Guide for the use of immunodiagnostic in sheep
applied to the epidemiological surveillance of
cystic echinococcosis
Guia para uso do imunodiagnóstico em ovinos
aplicado à vigilância epidemiológica da
equinococose cística
Poggio TV1, Mujica G2, Prada J3, Larrieu E4
1 Instituto de Ciencia y Tecnología César Milstein (CONICET), Saladillo 2468 (C1440FFX) –Buenos
Aires, Argentina.
2 Salud Ambiental Bariloche Ministerio de Salud, Provincia de Río Negro, Laprida 240 Viedma,
Argentina.
3 Faculty of Health and Medical Sciences, University of Surrey, Guildford, UK.
4 Instituto de Zoonosis. Facultad de Ciencias Veterinarias, Universidad Nacional de La Pampa, calle 5
esq. 116 General Pico, Argentina.
Correo electrónico: poggio69@gmail.com
RESUMEN La equinococosis quística (EQ) es una zoonosis parasitaria causada
por Echinococcus granulosus sensu lato. Técnicas inmunodiagnósticas
como Western blot (WB) o el enzimoinmunoensayo (ELISA), con distintos
antígenos, pueden ser aplicadas al diagnóstico de la EQ ovina
con fin tales de vigilancia epidemiológica en programas de control. Sin embargo, hay limitación para su uso por la existencia de reacción
cruzada antigénica entre diferentes especies de taeniidaes presentes
en el ovino. A pesar de ello se ha postulado la utilidad de establecer
sistemas de vigilancia basados en la identificación de infección presente
en un establecimiento ganadero, a lo que se denomina Unidad
Epidemiológica (UE). Una nueva técnica diagnóstica de ELISA ha sido
desarrollada y validada utilizando el antígeno EgAgB8/2 recombinante,
para detección de anticuerpos contra E. granulosus, estimándose
una DO 0.496 como el valor de corte que optimiza la sensibilidad y
especificidad. Para la determinación de la infección en UE se construyó un modelo bayesiano ejecutado con un algoritmo de cadena
de Markov Monte Carlo que permitió definir los tamaños de muestra
para diferentes prevalencias esperadas para asegurar que al menos
dos de las muestras sean verdaderamente positivas. De tal forma, el
sistema puede ser usado para identificar la prevalencia de la infección
en el área bajo control medida como porcentaje de UE con ovinos infectados
(infección presente) o identificar individualmente las UE con
transmisión presente, dada por la existencia de corderos infectados,
sobre las que se deben intensificar las medidas de control.
Palabras clave: Equinococosis, Inmunodiagnóstico, Ovinos,
Vigilancia, Control
ABSTRACT Cystic echinococcosis (CE) is a parasitic zoonosis caused by
Echinococcus granulosus sensu lato. Immunodiagnostic techniques
such as Western blot (WB) or enzyme-linked immunosorbent assay
(ELISA), with different antigens, can be applied to the diagnosis of CE
sheep for epidemiological surveillance purposes in control programs.
However, its use is limited by the existence of antigenic cross-reactivity
between different species of taeniidae present in sheep. Despite
this, the usefulness of establishing surveillance systems based on the
identification of infection present in a livestock establishment, known
as the Epidemiological Unit (UE), has been postulated. A new ELISA
diagnostic technique has been developed and validated using the recombinant
EgAgB8/2 antigen for the detection of antibodies against
E. granulosus, estimating an OD 0.496 as the cut-off value that optimize
diagnostic sensitivity and specificity. To determine the infection
in the EU, a Bayesian model was built, executed with a Monte Carlo
Markov chain algorithm, which allowed defining the sample sizes for
different expected prevalences to ensure that at least two of the samples
are truly positive. In this way, the system can be used to identify the prevalence of infection in the area under control measured as a
percentage of EU with the presence of infected sheep (infection present)
or individually identify the EU with present transmission, given
by presence of infected lambs, on which control measures should be
intensified.
Keywords: Echinococcosis, Immunodiagnostics, Sheep,
Surveillance, Control
RESUMO A equinococose cística (CK) é uma zoonose parasitária causada por
Echinococcus granulosus sensu lato. Técnicas de imunodiagnóstico
como western blot (WB) ou ensaio imunoenzimático (ELISA), com diferentes
antígenos, podem ser aplicadas no diagnóstico da DQ ovina
para fins de vigilância epidemiológica em programas de controle. No
entanto, seu uso é limitado pela existência de reação cruzada antigênica
entre diferentes espécies de taeniidae presentes em ovinos. Apesar
disso, postula-se a utilidade de estabelecer sistemas de vigilância baseados
na identificação de infecção presente em um estabelecimento
pecuário, conhecido como Unidade Epidemiológica (UE). Uma nova
técnica de diagnóstico ELISA foi desenvolvida e validada utilizando o
antígeno recombinante EgAgB8/2 para a detecção de anticorpos contra
E. granulosus, estimando uma DO 0,496 como valor de corte que
otimiza a sensibilidade e especificidade. Para determinar a infecção na
UE, foi construído um modelo Bayesiano, executado com um algoritmo
de cadeia de Monte Carlo Markov, que permitiu definir os tamanhos
das amostras para diferentes prevalências esperadas para garantir
que pelo menos duas das amostras sejam verdadeiramente positivas.
Desta forma, o sistema pode ser utilizado para identificar a prevalência
de infecção na área sob controle medida em porcentagem da UE
com ovinos infectados (infecção presente) ou identificar individualmente
a UE com transmissão presente, dada a existência de cordeiros
infectados, em quais medidas de controle devem ser intensificadas.
Palavras-chave: Equinococose, Imunodiagnóstico, Ovinos,
Vigilância, Controle
La equinococosis quística (EQ) es una zoonosis parasitaria causada
por Echinococcus granulosus sensu lato, parásito Cestoda, familia
Taeniidae. El ciclo de vida involucra a dos huéspedes mamíferos. Los
definitivos son carnívoros (especialmente perros) y los intermedios
son ungulados (siendo ovejas y cabras los de mayor importancia epidemiológica)(1).
El objetivo de la presente comunicación es describir una estrategia
para aplicar la serología ovina utilizando un novel antígeno recombinante
para la realización de pruebas de ELISA para la vigilancia epidemiológica
de la EQ.
En tal sentido, la vigilancia de EQ en el marco de programas de
control está dirigida hacia los distintos huéspedes: humanos, perros
y ovinos y caprinos(2). El diagnóstico en ovinos y caprinos se puede
realizar macroscópicamente en salas de faena (3-5). Sin embargo, en la
mayoría de las zonas endémicas estas no existen y el abastecimiento
urbano suele ser efectuado en carnicerías locales sin infraestructura
ni inspección sanitaria. En áreas rurales, por su parte, lo habitual es
el sacrificio domiciliario para consumo personal o venta al menudeo.
Por ello, si bien la inspección post mortem es la técnica de elección, es
dificultoso o virtualmente imposible basar el sistema de vigilancia en
esta fuente de datos
Además, el diagnóstico macroscópico en corderos tiene falsos negativos
(pueden no ser detectadas infecciones recientes o no ser observados
quistes hidatídicos pequeños recientemente formados). En
animales de varios años de edad por su parte, puede haber falsos positivos
(presencia de quistes supurados o calcificados debido a otras
infecciones o afecciones) (4).
Técnicas inmunodiagnósticas como western blot (WB) o el enzimoinmunoensayo
(ELISA), con distintos antígenos, pueden ser aplicadas
al diagnóstico de la EQ ovina (3,5,6-7). Sin embargo, hay limitación
para su uso en el ovino en tanto las infecciones por parásitos cestodos
distintos del E. granulosus (T. hydatigena, Monezia, Taenia ovis, Taenia
multiceps) son comunes en ovejas y cabras, existiendo evidencia de
reactividad cruzada antigénica entre las diferentes especies de taeniidae
(2,5-6).
UTILIDAD DE LAS PRUEBAS DIAGNÓSTICAS EN OVINOS
Se ha postulado la utilidad de establecer sistemas de vigilancia basados
en la identificación de infección presente en un establecimiento
ganadero, a lo que se denomina Unidad Epidemiológica (UE), en lugar de la estimación del porcentaje de perros parasitados tradicionalmente
utilizado. (8) El mismo criterio podría ser aplicado para identificar:
a. UE con transmisión presente de EQ basado en la presencia de
corderos infectados con E. granulosus.
b. UE con EQ basado en la presencia de ovinos de cualquier categoría
infectados.
c. Ovinos con EQ en rebaños que ingresaran a áreas libres de
infección.
Uso en sistemas de vigilancia epidemiológica posibilitaría:
a. Identificar las UE donde la transmisión se mantiene a pesar de
las medidas de control, para intensificar acciones sobre ellas.
b. Establecer la tendencia de la EQ en el área bajo programa estimando
anualmente (o periódicamente) el porcentaje de UE con
corderos infectados
c. Establecer el diagnóstico inicial de la prevalencia de EQ en la
majada ovina.
Finalmente, los programas de control contra EQ no tienen ningún
interés en el diagnóstico individual de infección por E. granulosus en
tanto se carece de tratamientos específicos validados y asimismo, porque
el interés epidemiológico es la determinación de la infección en el
rebaño.
Para utilizar el inmunodiagnóstico en el ovino con fines de vigilancia
se requiere
a. Contar con técnicas serológicas validadas.
b. Ajustar los tamaños de las muestras de animales a ser estudiados
para eliminar o disminuir los sesgos dados por las reacciones
cruzadas con otros cestodos.
INMUNODIAGNÓSTICO EN OVINOS
La supervivencia de E. granulosus depende de mecanismos de evasión eficientes que operan hacia el desarrollo de un quiste hidatídico. (1,2,6) De tal manera, el desarrollo de pruebas inmunodiagnósticas para tamizaje destinadas a la detección de E. granulosus depende de la interacción entre el hospedador y el parasito parásito durante el curso de la infección.ESTIMACIÓN DEL TAMAÑO DE LA MUESTRA
Para la determinación de la infección en UE se construyó un modelo
bayesiano ejecutado con un algoritmo de cadena de Markov Monte
Carlo (11) que permitió definir los tamaños de muestra para diferentes
prevalencias esperadas para asegurar que al menos dos de las muestras
sean verdaderamente positivas.
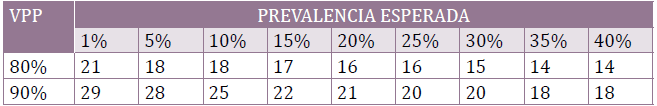
En la tabla 1 se presentan los tamaños de muestra que se deben
obtener para distintas prevalencias esperadas para valores predictivos
positivos de 80% y 90% (recomendable), bajo la premisa que el
tamaño de la muestra no depende del número de animales de la majada
sino fundamentalmente de la prevalencia esperada, que surge de
nuestro conocimiento de la epidemiologia local y de antecedentes bibliográficos
o reportes de estudios comparables. (13)
Tabla 1. Referencia para estimación de los tamaños de muestra de acuerdo a la
prevalencia esperada para identificar transmisión presente con un valor de corte
de 0.496, en función del valor predictivo positivo (VPP) deseado. Para prevalencias
esperadas superiores a 40%, se recomienda usar el tamaño de muestra
estimado para el 40%.
Obtención de muestras séricas e interpretación de resultados
Definido el tamaño de la muestra se seleccionarán aleatoriamente
los animales a ser estudiados.
La UE podrá estar constituida por:
a. Un solo establecimiento ganadero con un número de cabezas de
ganado suficiente para cubrir el muestreo.
b. En caso de pequeños productores con escaso número de animales
se podrá repartir la muestra entre varios productores
(por ejemplo, en el caso de reservas de población originaria que
comparten territorio).
En ovinos se obtendrá 10 cc. de sangre de la vena yugular, sujetos,
en posición de pie y con la cabeza fijada lateralmente, utilizando 25/8
y jeringas plásticas descartables.
Los tubos serán rotulados con un número que identifique al animal
(en caso de animales sin identificación, números sucesivos a partir del
1) y uno que identifique al productor. Los datos se volcarán en una
planilla de registro que deberá contener los números citados, el nombre
del productor, el área geográfica (georreferenciada) y la fecha de
obtención. Se deberán registrar asimismo el número total de ovinos
existentes y el número total de corderos.
El suero se extraerá mediante centrifugación, se conservará refrigerado
a 5º/8 ºC hasta su remisión a laboratorio (48 hs. máximo) en
donde se mantendrá en freezer a – 20 ºC hasta su procesado.
Interpretación de resultados: dos ovinos con valores serológicos
superiores al valor de corte DO 0.496 será indicativo de infección presente
(si se trata de masa ovina) o reciente (si se trata de corderos).
Los sistemas modernos de vigilancia de la EQ en animales tienen
como objetivo:
a. Identificar la prevalencia de la infección en el área bajo control
medida como porcentaje de UE con presencia de ovinos infectados
(infección presente) con posibilidades de transmitir la
infección a los perros y subsecuentemente a las personas, constituyendo
una línea base sobre la cual evaluar la tendencia de
la enfermedad en función de las medidas de control aplicadas.
b. Identificar individualmente las UE con transmisión presente,
dada por la presencia de corderos infectados, sobre las que se
deben intensificar las medidas de control, generalmente basadas
en la desparasitación de perros con praziquantel o mediante
la vacunación de ovinos con EG95.
De tal forma el ELISA en ovinos puede ser utilizado, solo o asociado
al tradicional CoproELISA en perros (2,8) u otras técnicas diagnósticas
en el huésped definitivo, como una nueva herramienta de vigilancia de
la EQ en forma estandarizada al servicio de los programas de control.
Ambos ofrecen ventajas logísticas porque las muestras se pueden
obtener con el mismo personal, los resultados de ambos sistemas pueden
complementarse y, finalmente, ambas técnicas son sencillas, económicas
y accesibles a países con pocos recursos y tecnología limitada
en sus laboratorios pudiendo ser utilizadas para la identificación de la
existencia de transmisión de E. granulosus y ajustar en consecuencia
las medidas de control.
1. Thompson RCA, McManus D. Aetiology: parasites and life cycles. In: Eckert J, Gemmel M, Meslin F, Pawlowsk,i Z. WHO/OIE Manual on Echinococcosis in Humans and Animals: a public health problem of global concern. WHO/OIE. France. 2001; p. 1-10.
2. Craig PS, Hegglin D, Lightowlers MW, Torgerson PR, Wang Q. Echinococcosis: Control and Prevention. In: Thompson, R.C.A., Deplazes, P., Lymbery, A. J., (Eds.), Echinococcus and Echinococcosis, 2017; Part B, pp. 55–158.
3. Moro P, Verastegui M, Gilman RH, Falcon N, Bernal T, et al. Enzyme-linked immunotransferblot assay for diagnosis of hydatidosis (Echinococcus granulosus) in sheep. Vet. Rec. 1997; 140, 605–606.
4. Cabrera PA, Irabedra P, Orlando D, Rista L, Harán G, et al. National prevalence of larval echinococcosis in sheep in slaughtering plants Ovis aries as an indicator in control programmes in Uruguay. Acta Trop. 2003; 85(2):281-5.
5. Craig P, Mastin A, van Kesteren F, Boufana B. Echinococcus granulosus: epidemiology and state-of-the-art of diagnostics in animals. Vet. Parasitol. 2015; 213:132e148.
6. McManus DP. Immunodiagnosis of sheep infections with Echinococcus granulosus: in 35 years where have we come? Parasite Immunol. 2014; 36(3):125-30.
7. Gatti A, Alvarez AR, Araya D, Mancini S, Herrero E, et al. Ovine echinococcosis. I. Immunological diagnosis by enzymeimmunoassay. Vet. Parasitol. 2007; 143:112–121.
8. Guarnera EA, Santillan G, Botinelli R, Franco A. Canine echinococcosis: an alternative for surveillance epidemiology. Vet Parasitol. 2000; 88(1-2):131-4.
9. Lamberti R, Cavagion L, Gatti A, Calvo C, Gino L, Puches VV, et al. Humoral response and evolution of Echinococcus infection in experimentally infected sheep. Rev. Bras. Parasitol. Vet. 2014; 23(2),237-40.
10. Larrieu E, Alvarez AR, Gatti A, Mancini S, Bigatti R, et al. Fisiopatología y respuesta inmune de ovinos experimentalmente infectados con Echinococcus granulosus. Medicina (B. Aires). 2009; 69(3),341-346.
11. Sykes AI, Larrieu E, Poggio TV, Céspedes G, Mujica G, et al. Modelling diagnostics for Echinococcus granulosus surveillance in sheep using Latent Class Analysis: Argentina as a case study. One Health. 2021; 4,14:100359
12. Poggio TV , Gómez JM , Boado LA , Vojnov AA, Larrieu E, Mujica GB, et al. Immunodiagnosis of cystic echinococcosis in livestock: Development and validation dataset of an ELISA test using a recombinant B8/2 subunit of Echinococcus granulosus sensu lato. Data in Brief 42 (2022) 108255.
13. Larrieu E. Manual de Epidemiologia y Salud Pública Veterinaria. Editorial UNRN, Rio Negro, Argentina. 2021; 181pp.
Fecha de recepción del artículo: 30/03/2022
Fecha de aceptación para su publicación: 08/06/2022