 Esta obra se publica bajo licencia Creative Commons 4.0 Internacional. (Atribución-No
Comercial-Compartir Igual) a menos que se indique lo contrario, http://www.creativecommons. org.ar/licencias
Esta obra se publica bajo licencia Creative Commons 4.0 Internacional. (Atribución-No
Comercial-Compartir Igual) a menos que se indique lo contrario, http://www.creativecommons. org.ar/licenciasDOI: http://dx.doi.org/10.19137/cienvet-201921105
 Esta obra se publica bajo licencia Creative Commons 4.0 Internacional. (Atribución-No
Comercial-Compartir Igual) a menos que se indique lo contrario, http://www.creativecommons. org.ar/licencias
Esta obra se publica bajo licencia Creative Commons 4.0 Internacional. (Atribución-No
Comercial-Compartir Igual) a menos que se indique lo contrario, http://www.creativecommons. org.ar/licencias
ARTÍCULO DE INVESTIGACIÓN
Dirofilariasis canina: una parasitosis emergente favorecida por el cambio climático
Canine dirofilariasis, an emerging parasitism favoured by climate changes
Cazaux, N.1; Meder, A.R.1; Calvo, C.2; Bertoldi, G.1, Miguel, C.1, Harfield, L.1
1Hospital Escuela de Animales Pequeños.
2Cátedra de Parasitología y Enfermedades Parasitarias. Facultad de Ciencias Veterinarias
de la Universidad Nacional de La Pampa. Calle 116 esq. 5. General Pico. La Pampa.
Argentina. CP 6360.
Correo electrónico: naticasaux@hotmail.com
Resumen: Dirofilaria immitis es una parasitosis zoonótica producida por un
nematodo responsable de generar en los animales infectados, enfermedad
cardiopulmonar, potencialmente mortal. La dirofilariosis se
presenta en zonas cálidas, con humedad, en el cual se encuentra el vector
responsable de su transmisión¸ el mosquito. A pesar de su denominación,
es una enfermedad principalmente pulmonar, afectándose la
parte cardíaca en fases avanzadas. Posee distintos estadíos larvarios,
pero es el estadio L3 el que resulta infeccioso, ingresa al huésped a
través de la picadura del vector y comienza a desarrollarse hasta los
estadios adultos que se ubican a nivel de las arterias pulmonares. El
principal hospedador definitivo y reservorio es el perro, pero puede
afectar a otros cánidos silvestres como el zorro. Los signos clínicos
van desde intolerancia al ejercicio, tos, crepitaciones respiratorias y a
medida que avanza y aumenta la carga parasitaria, hemoptisis o epistaxis,
pérdida de peso, sincopes, otros. Para arribar a su diagnóstico
es fundamental la detección de microfilarias, ya sea por extendidos
sanguíneos, en tubos de microhematocrito o por el test de Knott. Su
tratamiento consiste en eliminar las filarias jóvenes mediante administración
de lactonas macrocíclicas. Luego de lo cual se selecciona
como fármaco adulticida la melarsomina diclohidrato. Los cambios
climáticos acontecidos en el último tiempo preocupan debido a su
propagación hacia el norte de la Patagonia, y particularmente a nuestra
provincia de La Pampa.
Palabras Clave: Caninos ; Parasitosis ; Zoonosis ; Dirofilaria
Abstract:
Dirofilaria Immitis is a zoonotic parasitosis produced by a nematode
responsible for generating, in infected animals, potentially fatal cardiopulmonary
disease. The dirofilariosis occurs in warm areas, with
moisture, beeing the mosquito the vector responsible for its transmission.
Despite its denomination, it is a mainly pulmonary disease, affecting
the cardiac part in advanced stages. It has different larval stages,
but stage L3 is infectious. It enters the host through the vector bite
and begins to develop to adult stages which are located at the pulmonary
arteries. The main definitive host and reservoir is the dog, but it
can affect other wild canids like the fox. The clinical signs range from
exercise intolerance, coughing, respiratory crackles and as the parasitic
load progresses and increases, hemoptysis or epistaxis, weight loss,
syncopes, may occur. In order to arrive at its diagnosis, the detection
of microfilariae is essential, whether by taking blood smears from microhematocrit
tubes or by the Knott test. Its treatment consists in, the
elimination of the young filariae by the administration of macrocyclic
lactones and then the use of an adulticide drug, melarsomine diclohydrate.
The climatic changes that have occurred in the last time are of
concern due to their propagation towards the north of Patagonia, and
particularly to our province of La Pampa.
Key words: Canine ; Parasitism ; Zoonoses ; Dirofilaria
La dirofilariosis en una enfermedad cosmopolita y de distribución
mundial; las prevalencias más elevadas se localizan en zonas que mantienen
elevada temperatura y humedad durante, al menos, una parte
del año, de manera que estas condiciones ambientales favorezcan el
desarrollo y mantenimiento de poblaciones de mosquitos vectores[1].
En Argentina, la dirofilariasis canina por D. immitis se extiende en 11
provincias: Salta, Formosa, Chaco, Misiones, Corrientes, Entre Ríos,
Santa Fe, Santiago del Estero, Córdoba, Mendoza y Buenos Aires[2]. Si
bien los registros de casos señalan a la ciudad de La Plata y sus alrededores
como el límite sur de distribución del parásito en Sudamérica,
los modelos teóricos basados principalmente en la temperatura sugieren
que existen las condiciones climáticas adecuadas para su transmisión
en el norte de la Patagonia[3]. Si bien en la provincia de La Pampa
no se han documentado casos clínicos, los principales factores climáticos
asociados a su ciclo biológico favorecen la propagación y extensión
de esta parasitosis.
En este sentido, la sinergia entre temperatura y humedad como
consecuencia agravada por las grandes inundaciones y la elevada densidad
de mosquitos vectores, son condicionantes para el desarrollo de
la misma. Sobre la base de lo expuesto, el objetivo del presente trabajo
es actualizar el conocimiento sobre este parasito potencialmente
patógeno para la población canina y el hombre y sumar aportes sustanciales
al Médico Veterinario para su diagnóstico y tratamiento. Por
otra parte, el Grupo de Investigación del Hospital Escuela de Animales
Pequeños y la Cátedra de Parasitología y Enfermedades Parasitarias de
la Facultad de Ciencias Veterinarias de la Universidad Nacional de La
Pampa están elaborando un proyecto de alcance regional para relevar,
de manera prospectiva, la incidencia y prevalencia de Dirofilariosis canina
en las canileras municipales de las principales localidades de la
zona norte de la provincia de La Pampa.
La infección causada por el nemátodo Dirofilaria immitis, tiene varias
denominaciones, como por ejemplo dirofilariosis, verminosis cardiaca,
enfermedad por gusanos cardiacos, enfermedad del gusano del
corazón o heartworm disease[4]. Al contrario de lo que se piensa por
su denominación, el parásito en su estado adulto reside principalmente
en las arterias pulmonares del huésped definitivo, manteniéndose
en ellas gracias a la circulación sanguínea y cuando ésta cesa, los vermes
caen al ventrículo derecho donde se encuentran en los exámenes
post mortem[5]. (Imagen 1)
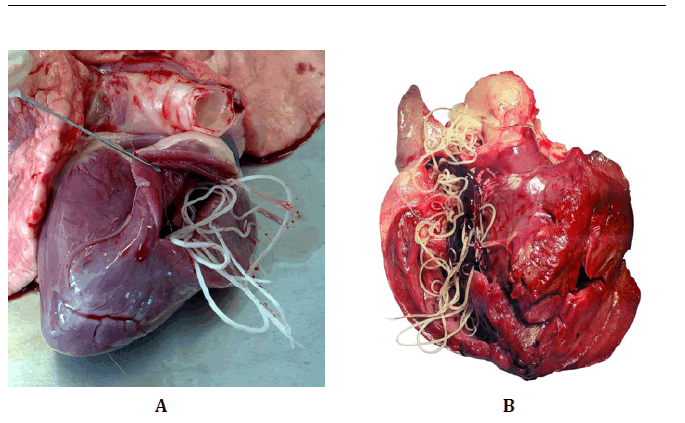
Imagen 1. Muestras anatomopatológicas cardiacas que permiten dimensionar
el tamaño de los vermes adultos de dirofilarias inmitis en corazones caninos
luego de la apertura de aurícula y ventrículo derecho. Fuente: http://patovet. com/o/tag/dirofilaria-immitis/ [6]
Es una enfermedad de transmisión vectorial ejercida por mosquitos
culícidos pertenecientes a los géneros Culex, Aedes, Anopheles, Culiseta
y Coquillettidia, entre otros[7]. El desarrollo de la etapa larvaria L1 a L3
puede ocurrir en varias especies diferentes de mosquitos, durante un
período de 30 a 60 días[8]. Durante el estadio larvario L3 infeccioso, las
larvas se transmiten a través de la inoculación en la piel del huésped
primario por el mosquito. Una vez que se han inoculado las larvas, se
desarrollan en la etapa L3 a L4 en el tejido subcutáneo durante un período
de aproximadamente 10 a 12 días. El desarrollo de L4 a L5 tiene
lugar en el tejido muscular de 50 a 70 días después de la inoculación[5].
Los gusanos juveniles (L5) penetran en las venas sistémicas y se transportan
a las arterias pulmonares, donde continúan desarrollándose en
gusanos adultos. En casos severos, las larvas también pueden entrar
en la cámara derecha del corazón y en la vena cava caudal, pero en la
mayoría de los casos el flujo de sangre retendrá las larvas en la arteria
pulmonar y sus ramas[9]. Las filarias hembras adultas son las responsables
de eliminar hacia la circulación periférica microfilarias, las
cuales ingresaran a un nuevo mosquito, para una nueva transmisión.
El período de prepatencia, lapso de tiempo entre el ingreso del parasito
hasta su madurez sexual, es de aproximadamente 6 meses, y los adultos pueden vivir entre 5 a 7 años, mientras que las microfilarias
liberadas a circulación tienen una vida media de 2 años (Imagen 2).
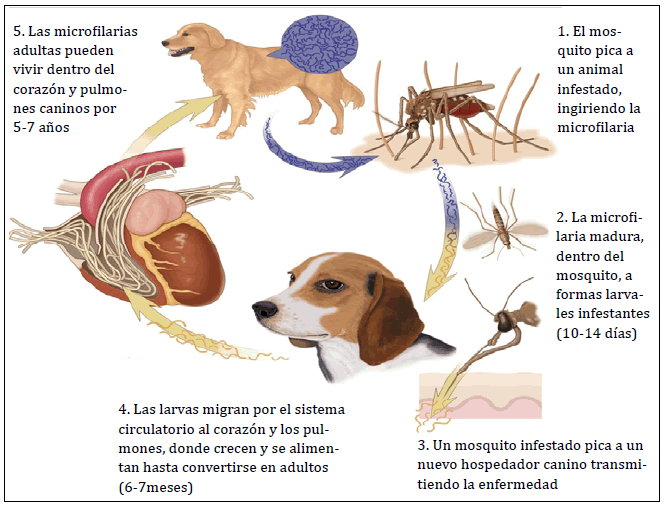
Imagen 2. Ciclo biológico de Dirofilaria Inmitis. En la ilustración se muestran
las distintas fases entre huéspedes intermediario y definitivo por las cuales
van pasando los distintos estadios de esta enfermedad parasitaria verminosa.
Fuente:http://www.veterinarioperu.com/filaria-canina/ [10]
El principal hospedador definitivo y reservorio de dirofilariosis
es el perro, pero otros cánidos silvestres tienen un importante rol en
la transmisión, como el zorro. Se puede establecer como factores de
riesgo para la infección, la especie animal (el perro es el huésped primario
natural); el sexo del huésped primario (los perros machos son
más vulnerables que las perras); el hábitat del huésped primario (los
perros que viven al aire libre están más expuestos a la infección); y el
tamaño del huésped primario (los perros grandes tienen más probabilidades
de infectarse que los perros pequeños)[11]. Los perros menores
de seis meses no pueden ser portadores de gusanos adultos, ya que pasan
aproximadamente seis meses desde el momento en que el perro se
infecta hasta que los gusanos del corazón se convierten en adultos. Por lo tanto, es poco probable que se observen signos clínicos en perros
menores de un año. Sin embargo en animales jóvenes con una masiva
primoinfección esta parasitosis suele tener una presentación aguda,
de curso rápido y mortal. Por otra parte la patología es más severa y
acelerada en perros activos comparado con perros inactivos, sea cual
sea la carga parasitaria. Los perros de razas pequeñas no toleran la
infestación parasitaria cardíaca tan bien como los de raza grande.[12]
Los gusanos del corazón afectan principalmente a los perros, pero
también se han identificado en una serie de otras especies animales,
incluidos gatos, zorros, hurones, leones marinos y perros salvajes. [9, 11]
Dirofilaria immitis produce numerosas lesiones orgánicas y en su
mayoría graves. A continuación se mencionan algunas: [1, 5]
• Arteritis pulmonar proliferativa
• Hipertensión pulmonar
• Insuficiencia cardiaca congestiva derecha
• Congestión hepática crónica
• Síndrome de la vena cava
• Síndrome Nefrótico (amiloidosis o glomérulonefritis como consecuencia
de inmunocomplejos)
Como anteriormente se mencionó, la manifestación de los signos
clínicos asociados a la dirofilariosis refleja la carga parasitaria de parásitos
adultos, la duración de la infestación, y la interacción huésped-
parásito[12]. Inicialmente, la infección no presenta sintomatología
y esta empieza a mostrarse en cuadros avanzados de la enfermedad.
Los síntomas van apareciendo progresivamente y generalmente no se
hacen evidentes hasta pasados varios años desde la infección[13].
Muchos perros son totalmente asintomáticos teniendo altas cargas
parasitarias o presentan signos tan discretos que resulta difícil diagnosticarlos.
Los signos clínicos de la enfermedad del gusano del corazón
se atribuyen al daño causado en las arterias pulmonares y en
el lado derecho del corazón; sin embargo, las larvas también pueden
propagarse a otros órganos, como los ojos, los riñones, el sistema nervioso
central y el tejido subcutáneo[13]. Los perros con dirofilariosis,
de moderada a avanzada, presentan intolerancia al ejercicio, tos, disnea,
y crepitaciones respiratorias. Si el daño es severo, la tromboembolia
pulmonar causa hemoptisis. Se puede ver antes, pero ocurre más a menudo después del tratamiento adulticida [12]. La hemoptisis y/o
epistaxis aparecen ante aneurismas y la presencia de tos lleva a la rotura
de los vasos. [1] El síncope está asociado a un daño severo de
la arteria pulmonar y a hipertensión pulmonar. [12]. Otros signos que
se pueden apreciar son letargia, apatía, pérdida de peso y ascitis con
efusión pleural. La auscultación cardiaca generalmente es normal, sin
embargo en aquellos pacientes con síndrome de vena cava o con insuficiencia
cardiaca derecha, se puede apreciar un soplo cardiaco sistólico [1].
En los pacientes con síndrome de vena cava, se presenta de forma
brusca un choque precordial, con taquicardia, taquipnea y disnea. En
dichos casos se denomina migración retrógrada, al desplazamiento de
los parásitos desde las arterias pulmonares hasta el ventrículo derecho[5]. Se produce en animales que presentan una elevada carga parasitaria,
encontrándose gran parte de los parásitos en las venas cavas
craneal, caudal y aurícula derecha. [1] Si la masa de vermes es lo bastante
grande o si se entrelazan unos con otros alrededor de la válvula,
las fuerzas hemodinámicas pueden no ser suficientes para expulsarlos
del corazón.[5] Como resultado, hay una disminución del flujo sanguíneo
sistémico dando síntomas de mala perfusión y shock cardiocirculatorio. [1]
1. Detección de microfilarias:
• Extendidos sanguíneos: Efectivo en los casos en que haya
más de 1.000 microfilarias por mililitro de sangre. Método
sencillo donde se extiende una gota de sangre sobre un portaobjetos
y se observa a 100 aumentos.
• Tubo de microhematocrito: Las larvas se sitúan justo encima
de la capa de leucocitos.
• Test de Knott: Método con mayor índice de detección. El mismo
consiste en mezclar 1cc de sangre con 9 cc de una solución
de formol al 2%. Centrifugar al 1.500 r.p.m. durante 5
minutos. El sedimento es lo que se utiliza, se mezcla a partes
iguales con nuevo azul de metileno al 0,1%. Una gota de este
sedimento y se observa entre porta y cubre. Estas pruebas
son indicadas cuando son pacientes sintomáticos o microfilaremicos,
de otra manera arroja falsos negativos.
2. Test ELISA para la detección de antígeno filarial: test de
elección para el diagnóstico de esta enfermedad. Indicado especialmente en aquellas infecciones ocultas o perros amicrofilaremicos,
ya que presentan una especificidad elevada.
3. Radiología Torácica: Método útil para estimar la gravedad de
la infestación. Con esta técnica diagnóstica se pueden observar
las ramas interlobares de la arteria pulmonar agrandadas y tortuosas,
grados variables de enfermedad pulmonar parenquimatosa,
cardiomegalia a predominio derecho, desplazamiento traqueal
hacia dorsal y edema pulmonar cardiogénico (Imagen 3).
4. Ecocardiografía: Muy útil para confirmar el diagnóstico de
síndrome de vena cava en perros con ascitis. Algunos de los
hallazgos ecográficos que nos hacen sospechar de esta enfermedad
son dilatación de la arteria pulmonar, dilatación e hipertrofia
del ventrículo derecho, aplanamiento septal, entre otros
(Imagen 4).
5. Electrocardiografía: No es un método que arroja datos significativos
por sí mismo, sin embargo, asociado a otros estudios,
colabora sustancialmente en el diagnóstico de la patología en
casos avanzados. Los hallazgos muestran sobrecarga cameral
ventricular derecha asociada a patrón S en derivaciones I, II y
aVF [1, 12]. (Imagen 5).
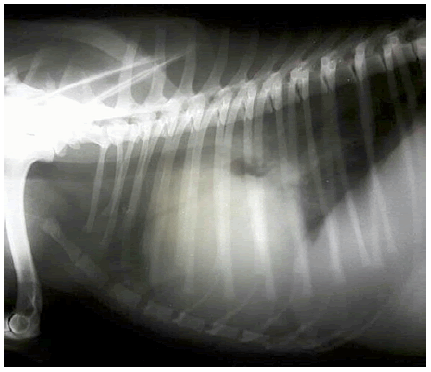
Imagen 3. Placa radiológica LLD de un paciente canino Cocker spaniel de 7 años de edad.
En la imagen se puede observar cardiomegalia generalizada a predominio del ventrículo
derecho (corazón mayor a 4 espacios intercostales y recostado ampliamente sobre el
esternón), elevación traqueal y paralelismo con la columna vertebral toráxica y patrón
alveolar perihiliar en relación a carina bronquial y paquete vasculobronquial apical.
Cortesía Dr. Jorge Musitani. Trenque Lauquen. Provincia de Buenos Aires. Argentina.
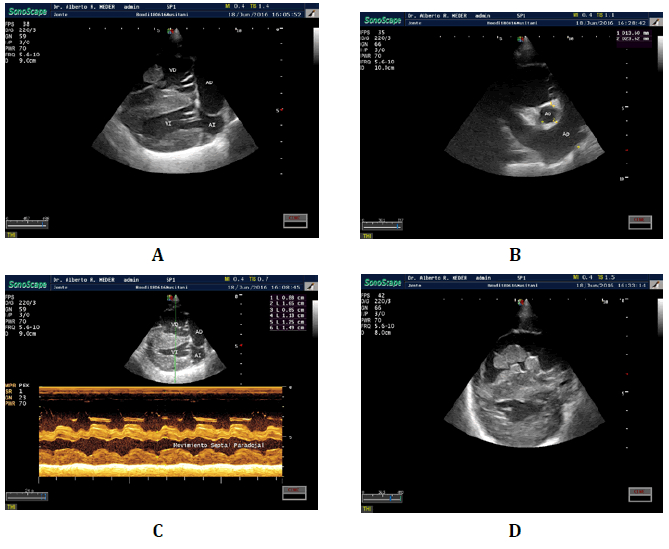
Imagen 4. Estudio ecocardiográfico. A. Eje largo 4 cámaras donde se aprecia
hipertrofia septal, sobrecarga de volumen de atrio izquierdo y presencia de una
nodulación en relación a cuerdas tendinosas (flecha). B. Eje corto tracto de salida
del ventrículo derecho donde se aprecia el aumento de diámetro del tronco
pulmonar y una relación aorta/pulmonar significativamente alterada. C. Eje
largo 4 cámaras y modo M simultáneo que muestra la hipertrofia septal y movimiento
paradojal del mismo asociado a sobrecarga de volumen y presión. D. Eje
corto nivel cuerdas tendinosas que muestra la hipertrofia septal y nodulaciones
asociadas a la misma y a las cuerdas tendinosas (flecha).
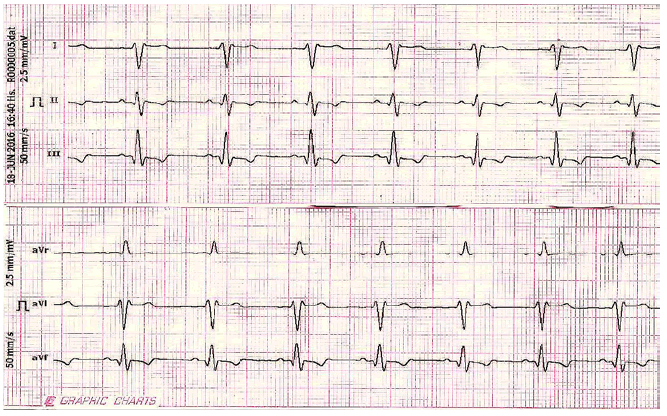
Imagen 5. Registro electrocardiográfico que muestra la presencia de Patrón S en derivaciones
I, II y aVF. Se evidencia un ritmo sinusal, ondas S profundas y sobrecarga cameral
atrial derecha. El registro se realizó a 2.5mm/mV y a 50 mm/seg.
Antes de comenzar con el tratamiento es necesario establecer la
gravedad del paciente. En función de la sintomatología y los resultados
obtenidos en las pruebas diagnósticas, la dirofilariosis se ha clasificado
tradicionalmente en cuatro clases o niveles de gravedad [1].
En la actualidad se prefiere una clasificación más simple, que separa
a los pacientes en dos categorías en función del riesgo de producirse
tromboembolismos pulmonares durante el tratamiento adulticida [14]:
1. Bajo riesgo de complicaciones tromboembólicas. Se trata de
animales con baja carga parasitaria y sin lesiones de la vasculatura
o parénquima pulmonar.
2. Riesgo elevado de complicaciones tromboembólicas.
Antes de eliminar las filarias adultas, se debe eliminar las larvas
migratorias L3 y L4. Esto es debido a que el único fármaco adulticida
disponible (melarsomina diclorhidrato) no puede eliminar filarias
menores de 4 meses de edad. Por lo tanto, primero deben eliminarse
las larvas menos de 60 días mediante la administración mensual de
lactonas macrocíclicas a dosis preventivas durante 2 meses previo al
tratamiento adulticida mientras que las larvas mayores de 60 días no susceptibles al fármaco preventivo alcanzarán la edad suficiente para
ser sensibles a la melarsomina [13].
La melarsomina diclorhidrato es el único fármaco adulticida autorizado
en la actualidad. Se administra mediante inyección intramuscular
profunda en la musculatura lumbar. Se recomienda el tratamiento
denominado “diferido”. El mismo consiste en aplicar una primera inyección
de melarsomina (2,5 mg/kg), una segunda inyección al cabo
de un mínimo de 30 días (2,5 mg/kg) y una tercera inyección pasadas
las 24hs de la aplicación anterior (2,5 mg/kg). Esta eliminación
progresiva minimiza el riesgo de tromboembolismo producido por la
muerte de los parásitos y permite al organismo eliminar los fragmentos
embólicos de forma más segura, lo que resulta en complicaciones
pulmonares menos severas y frecuentes [1].
El confinamiento estricto del paciente es esencial durante 4-6 semanas
post-tratamiento. La demanda de flujo reducido a través de las
arterias pulmonares es beneficioso para reducir el daño endotelial y
para promover la reparación vascular.
En aquellos pacientes con altas cargas parasitarias o con síndrome
de vena cava, la retirada quirúrgica es el único tratamiento agudo recomendado
[12].
Habiendo expuesto las distintas características y particularidades
de esta parasitosis, y debido a los cambios climáticos acontecidos en la
provincia de la Pampa, es importante que como Médicos Veterinarios
tengamos a esta enfermedad dentro de nuestros diagnósticos diferenciales.
Cuando llega un paciente a consulta, con sospechas de dirofilariosis
son varios las consideraciones que hay que tener en cuenta:
1) en primer lugar, determinar mediante una correcta anamnesis si
pertenece o estuvo en algún momento en alguna zona endémica, o si
el lugar ha sido afectado últimamente por inundaciones, 2) si presenta
signos clínicos tales como intolerancia al ejercicio, tos, disnea, entre
otros, compatibles con el cuadro clínico de un paciente infectado, 3)
una vez que se logra confirmar el diagnóstico, por medio de las distintas
pruebas descriptas anteriormente, es importante determinar
frente a qué paciente nos enfrentamos, es decir paciente de bajo riesgo
o riesgo elevado, 4) y por último instaurar el tratamiento adecuado
para cada caso.
1. Carretón Gómez E., Falcón Cordón Y., Montoya Alonso J.A. y Garcia Guasch L. Manual de Enfermedades Respiratorias en Animales de Compañía. Gráfica IN-Multimédica S.A. 2016; 305-324
2. Vezzani D., Eiras DF., Wisnivesky C. Dirofilariasis in Argentina: Historical review and first report of Dirofilaria immitis in a natural mosquito population. Veterinary Parasitology: 2006; 136:259-273.
3. Cuervo PF., Rinaldi L., Cringoli G. Modeling the extrinsic incubation of Dirofilaria immitis in South America based on monthly and continuous climatic data. Veterinary Parasitology. 2015; 209:70-75.
4. Rawlings CA., Calvert CA. Tratado de Medicina Interna Veterinaria. Verminosis cardiaca. 4a ed. Buenos Aires. Argentina: Inter–Médica; 1997.
5. Kittleson MD., Kienle RD. Medicina cardiovascular de pequeños animales. 2a ed. Barcelona. España: Multimédica; 2000.
6. PatoVet.com. Perú: Dream Theme [actualizado 22 de Sept 2014; citado 8 de Febrero en 2019]. Disponible en http://patovet.com/o/tag/dirofilaria-immitis/.
7. Simón F., Siles LM., Morchón R., González Miguel J., Mellado Hernández I. Human and animal dirofilariasis: the emergence of a zoonotic mosaic. emmerging zoonosis. Clin. Microb. Rev. 2012; 25: 507-544.
8. Calvert CA, Rawlings CA, McCall JW. Canine heartworm disease. I: Fox PR, Sisson D, Moïse NS, eds. Textbook of canine and feline cardiology principles and clinical practice. 2nd ed. Philadelphia: Saunders, 1999:702-26.
9. Calvert CA, Thrall DE. Treatment of canine heartworm disease coexisting with right- side heart failure. J Am Vet Med Assoc 1982; 180:1201.
10. Veterinario Perú. VetHelp. Perú: Copyright ©; 2013 [actualizado 2 de May 2013; citado 8 en 2019]. Disponible en: http://www.veterinarias.org/filaria-canina/.
11. Kittleson MD. Heartworm infestation and disease (Dirofilariasis). In: Kittleson MD, Kienle RD, eds. Small animal cardiovascular medicine. St.Louis: Mosby, 1998: 370-401.
12. Montoya-Alonso J.A. y Garcia Guasch L. Manual de Enfermedades Respiratorias en Animales de Compañía. Gráfica IN-Multimédica S.A.2016. pp. 305-324
13. Carretón E., Morchón R., Montoya-Alonso J. A. Dirofilariosis cardiopulmonar canina. Dirofilariosis. Pautas de manejo clínico. 2012
14. McCall J. W., Genchi C., Kramer L. H., Guerrero J., Venco L. Heartworm disease in animals and hu mans. Advances in Parasitology, 2008; 66: 193-285.
Fecha recepciòn de artìculo: 10-08-2018
Fecha aceptación artículo: 12-03-2019